Answered step by step
Verified Expert Solution
Question
1 Approved Answer
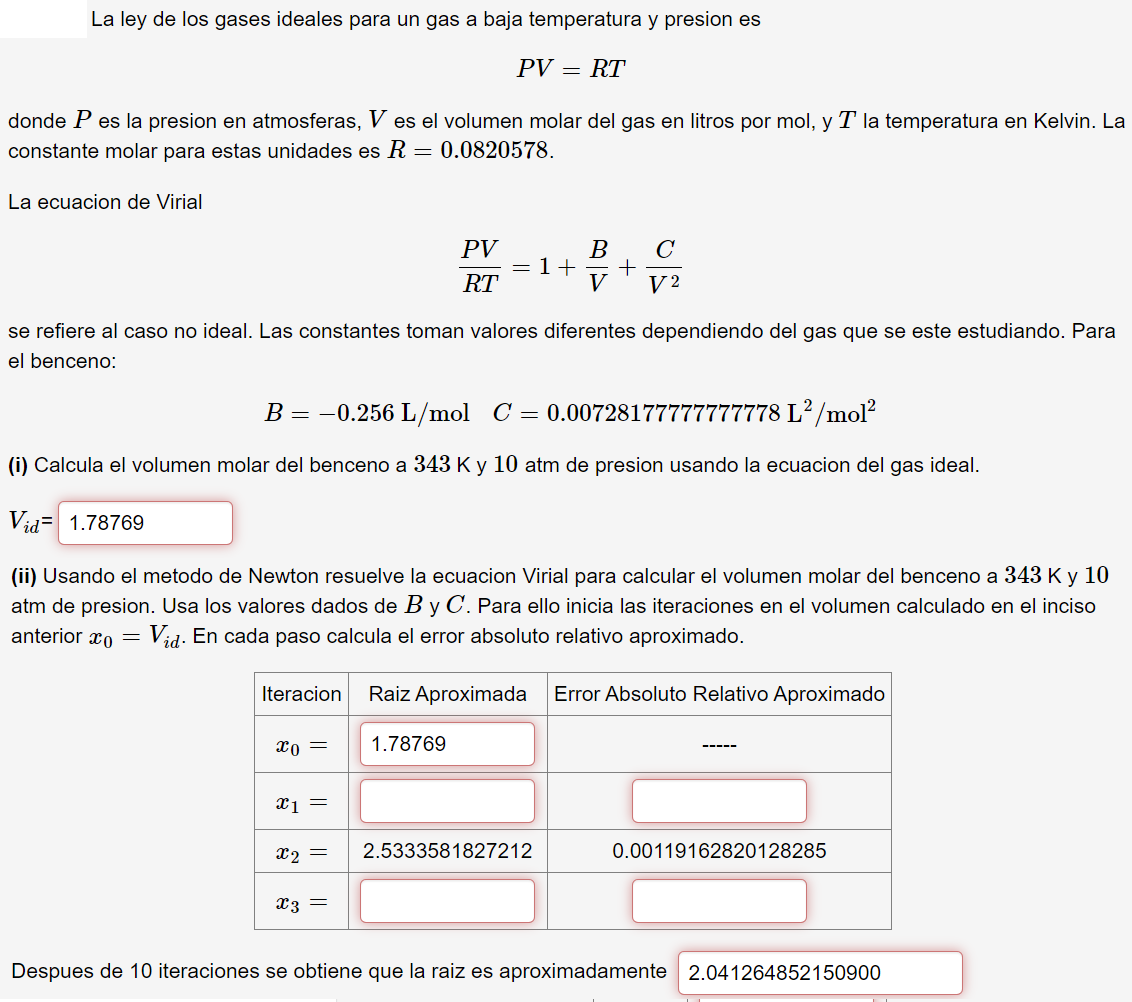
La ley de los gases ideales para un gas a baja temperatura y presion es P V = R T donde P es la presion
La ley de los gases ideales para un gas a baja temperatura y presion es
donde es la presion en atmosferas, es el volumen molar del gas en litros por mol, y la temperatura en Kelvin. La
constante molar para estas unidades es
La ecuacion de Virial
se refiere al caso no ideal. Las constantes toman valores diferentes dependiendo del gas que se este estudiando. Para
el benceno:
i Calcula el volumen molar del benceno a y atm de presion usando la ecuacion del gas ideal.
ii Usando el metodo de Newton resuelve la ecuacion Virial para calcular el volumen molar del benceno a y
atm de presion. Usa los valores dados de y Para ello inicia las iteraciones en el volumen calculado en el inciso
anterior En cada paso calcula el error absoluto relativo aproximado.
Despues de iteraciones se obtiene que la raiz es aproximadamente
POR FAVOR, resolver sin y con programa, necesito saber cmo se hace, de cualquier forma gracias!
Step by Step Solution
There are 3 Steps involved in it
Step: 1

Get Instant Access to Expert-Tailored Solutions
See step-by-step solutions with expert insights and AI powered tools for academic success
Step: 2

Step: 3

Ace Your Homework with AI
Get the answers you need in no time with our AI-driven, step-by-step assistance
Get Started


